《藥品技術轉讓注冊管理規定》解讀 技術轉讓的核心要點與流程

藥品技術轉讓是藥品上市許可持有人制度下的關鍵環節,對于優化資源配置、促進產業升級具有重要意義。國家藥品監督管理局頒布的《藥品技術轉讓注冊管理規定》(以下簡稱《規定》)為這一活動提供了明確的法規框架和操作指南。
一、 技術轉讓的定義與范疇
《規定》明確,藥品技術轉讓是指藥品技術的所有者按照本規定的要求,將藥品生產技術轉讓給受讓方藥品生產企業,并由受讓方藥品生產企業申請藥品注冊的過程。這里的技術主要指藥品的處方、生產工藝、質量標準、質量控制方法以及相關的技術資料和知識產權。轉讓范圍通常包括新藥技術轉讓和已有國家藥品標準的藥品技術轉讓。
二、 轉讓雙方的基本條件
- 轉讓方(持有藥品批準證明文件者)應具備對轉讓技術的合法所有權或處分權,且該藥品批準文號必須有效。
- 受讓方(藥品生產企業)必須持有與轉讓藥品劑型相一致的《藥品生產許可證》和《藥品生產質量管理規范》(GMP)認證證書,并具備相應的生產條件、檢驗能力和質量保證體系。
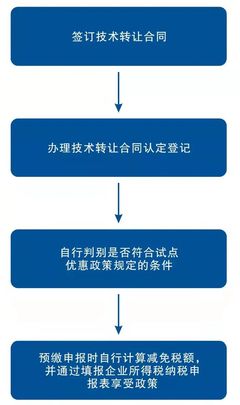
三、 技術轉讓注冊的核心程序
技術轉讓的注冊申請,本質上是受讓方就轉讓藥品申請新的藥品批準證明文件的過程。主要程序包括:
- 申請與受理:受讓方向所在地省級藥品監督管理部門提交技術轉讓注冊申請及相關資料。
- 現場核查與抽樣檢驗:藥品監督管理部門對受讓方的生產條件和試制現場進行核查,并對連續生產的3批樣品進行抽樣,送藥品檢驗機構檢驗。
- 技術審評:國家藥品監督管理局藥品審評中心基于申報資料、現場核查報告和樣品檢驗結果,對技術轉讓的可行性、受讓方產品質量的可控性與一致性進行科學審評。
- 審批與發證:審評通過后,由國家藥監局審批,符合規定的,發給新的藥品批準文號,并注銷轉讓方的原藥品批準文號。
四、 申報資料的關鍵要求
申報資料是審評的核心依據,必須全面、真實、規范。重點包括:
- 證明轉讓合法性的協議或合同。
- 轉讓藥品的批準證明文件復印件。
- 詳細的工藝驗證資料和質量對比研究資料,證明受讓方產品與原產品在質量、安全性和有效性上保持一致。
- 受讓方相關的資質證明文件(生產許可證、GMP證書等)。
五、 風險控制與監管重點
《規定》著重強調了技術轉讓過程中的質量風險控制。監管的核心在于確保技術轉移后,受讓方生產的產品質量與轉讓方原產品“等同”,不能因生產場地、設備、工藝參數的轉移而產生質量差異。因此,工藝驗證、持續穩定性考察以及嚴格的質量對比研究是成功通過技術審評的基石。
《藥品技術轉讓注冊管理規定》的出臺,規范了藥品技術轉讓行為,保障了技術轉讓過程中藥品質量的延續性和可控性。深入理解《規定》要求,扎實做好工藝驗證和質量研究,是順利完成技術轉讓、實現技術價值轉化的關鍵。這不僅是法規合規的要求,更是對公眾用藥安全負責的體現。
如若轉載,請注明出處:http://www.jqhnt.cn/product/76.html
更新時間:2026-05-08 10:45:53